Mundo
Microbioma intestinal dita sucesso de probióticos e abre caminho para terapias personalizadas
Estudo global com mais de 50 mil amostras revela por que bactérias benéficas como Bifidobacterium persistem em alguns indivíduos — e falham em outros —, inaugurando uma nova era de precisão na nutrição e na medicina
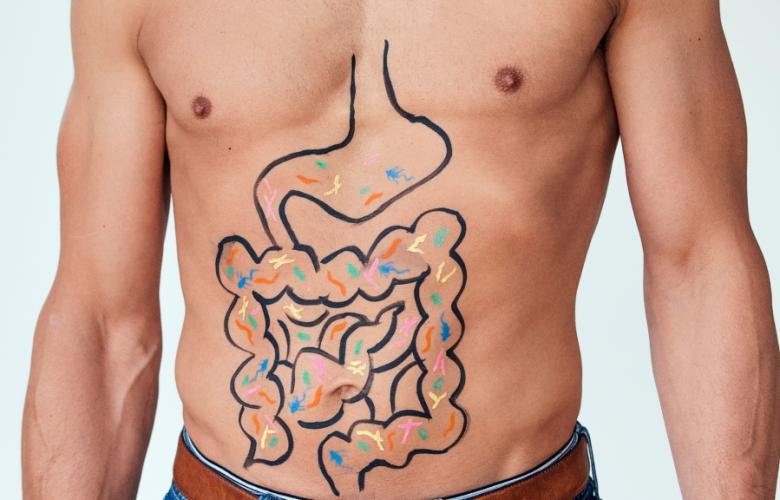
Imagem: Reprodução
Em um avanço que promete redefinir o uso de probióticos na prática clínica, um amplo estudo internacional publicado nesta quinta-feira (23), na revista Nature Communications, demonstra que a eficácia dessas bactérias “do bem” depende menos da dose ingerida e mais do ambiente intestinal de cada indivíduo. A pesquisa analisou 51.244 microbiomas humanos de 45 países e concluiu que o sucesso de colonização de espécies do gênero Bifidobacterium — amplamente utilizadas em suplementos — pode ser previsto com base na composição prévia da microbiota.
O trabalho, liderado por Sourav Goswami e Tarini Shankar Ghosh no Indraprastha Institute of Information Technology Delhi, com colaboração de cientistas da University College Cork e do All India Institute of Medical Sciences, oferece uma explicação robusta para um problema antigo: por que probióticos funcionam para alguns e não para outros.
“Durante anos, observamos resultados inconsistentes em ensaios clínicos com probióticos. Agora sabemos que isso não é aleatório — é uma questão de ecologia microbiana”, afirma Ghosh.
Um mapa global do intestino humano
A equipe compilou dados de 149 coortes, abrangendo diferentes faixas etárias, estilos de vida e condições de saúde. Ao cruzar essas informações, os pesquisadores identificaram padrões consistentes de interação entre Bifidobacterium e outras bactérias intestinais.
Entre os principais achados está a forte associação positiva entre Bifidobacterium e bactérias produtoras de butirato — um ácido graxo essencial para a saúde do cólon. Já a presença de microrganismos potencialmente patogênicos, como certos Firmicutes, mostrou correlação negativa com a colonização dessas bactérias benéficas.
“Não é apenas quem você adiciona ao microbioma, mas quem já está lá que determina o resultado”, explica Fergus Shanahan, coautor do estudo.
O “score” que prevê o sucesso
A inovação central da pesquisa é o desenvolvimento de um indicador chamado “Receptive Score” (índice de receptividade), que mede o quão favorável é o microbioma de uma pessoa para a colonização de um probiótico específico.
Esse índice combina dois fatores: a presença de microrganismos que favorecem ou inibem o crescimento de Bifidobacterium e a quantidade já existente dessa bactéria no intestino. Em testes com dados independentes de 1.633 microbiomas submetidos a intervenções com probióticos, o modelo previu corretamente o sucesso da colonização em 69,23% dos casos.
“É como prever se uma planta vai crescer: não basta plantar a semente, é preciso avaliar o solo”, resume Goswami.
Idade, estilo de vida e saúde influenciam
O estudo também revelou que a interação entre bactérias varia ao longo da vida. Em bebês, espécies como B. breve e B. bifidum dominam, impulsionadas pelo consumo de leite materno. Já em adultos, B. adolescentis se torna mais prevalente — e também mais associada a perfis de microbioma considerados saudáveis.
Além disso, fatores como urbanização e dieta influenciam significativamente essas relações. Populações urbanas industrializadas apresentaram maior abundância de Bifidobacterium, enquanto comunidades rurais exibiram padrões distintos, com menor presença dessas bactérias.
Curiosamente, doenças como diabetes tipo 2, câncer colorretal e COVID-19 não alteraram de forma significativa os padrões de associação entre bactérias, sugerindo que essas interações são estruturalmente estáveis.
Implicações clínicas e comerciais
Os resultados têm implicações diretas para a indústria de suplementos e para a medicina personalizada. Hoje, probióticos são vendidos de forma padronizada, sem considerar o perfil individual do consumidor. Isso pode mudar.
“Estamos caminhando para uma era em que o probiótico certo será prescrito para a pessoa certa, no momento certo”, afirma Paul W. O’Toole, também autor do estudo.
Além disso, os pesquisadores observaram que indivíduos com maior “Receptive Score” apresentaram melhora em sintomas gastrointestinais e redução de marcadores inflamatórios em alguns ensaios clínicos, embora os dados ainda sejam preliminares.
A ecologia invisível que governa a saúde
O estudo reforça a visão do microbioma como um ecossistema complexo, onde cooperação e competição entre espécies moldam os resultados clínicos. Interações como o “cross-feeding” — em que uma bactéria produz nutrientes utilizados por outra — foram identificadas como mecanismos-chave para a estabilidade do sistema.
Imagem: Reprodução
Por exemplo, Bifidobacterium pode degradar açúcares complexos em moléculas simples que alimentam bactérias produtoras de butirato, criando um ciclo simbiótico que beneficia o hospedeiro.
Por outro lado, bactérias associadas a doenças competem por recursos essenciais, como metais, ou produzem compostos inflamatórios, dificultando a colonização de probióticos.
Apesar da escala inédita, os autores reconhecem limitações. A escassez de dados de populações não industrializadas e a ausência de informações detalhadas sobre dieta e medicamentos em muitos conjuntos de dados podem ter restringido algumas análises.
Além disso, o estudo foi conduzido em nível de espécie, não de cepa — uma distinção importante, já que diferentes cepas de uma mesma bactéria podem ter efeitos distintos.
“Precisamos agora validar esses achados em estudos clínicos controlados e integrar dados metabolômicos para entender os mecanismos em profundidade”, diz Ghosh.
Um novo paradigma
Ao demonstrar que o sucesso de probióticos pode ser previsto e potencialmente otimizado, o estudo inaugura um novo paradigma na saúde intestinal. Mais do que suplementos genéricos, o futuro aponta para intervenções personalizadas baseadas no perfil microbiano de cada indivíduo.
Em um mundo onde doenças crônicas e inflamatórias estão em ascensão, compreender — e modular — o ecossistema invisível que habita o intestino pode ser uma das chaves mais promissoras da medicina do século XXI.
Referência
Goswami, S., Ansari, A., Saraf, C. et al. Características do microbioma intestinal associadas à colonização por Bifidobacterium predizem padrões personalizados de persistência de probióticos. Nat Commun (2026). https://doi.org/10.1038/s41467-026-72289-9